Contenidos en este artículo
Los dispositivos médicos deben pasar por un proceso de fabricación y calificación de equipos riguroso antes de ser introducidos en el mercado.
Es por ello que los fabricantes deben asegurarse de que los métodos y los equipos utilizados durante la elaboración. Se rijan por los controles adecuados para entregar productos seguros y que cumplan con los requisitos reglamentarios.
Cuando se trata de dispositivos médicos, la precisión en los procesos de fabricación es indiscutible. La calificación de equipos a través de estos procesos es clave para evitar fallas en los dispositivos y el retiro del producto del mercado.

Calificación de Equipos para Dispositivos Médicos
El Reglamento del Sistema de Calidad de la FDA y la norma ISO 13485 exigen que los fabricantes de dispositivos médicos verifiquen que sus productos cumplan con las especificaciones de diseño estipuladas.
En Chile, los dispositivos médicos se regulan bajo la Ley 19.497 y el Reglamento de Control de Productos y Elementos de Uso Médico D.S. Nº 825/98.
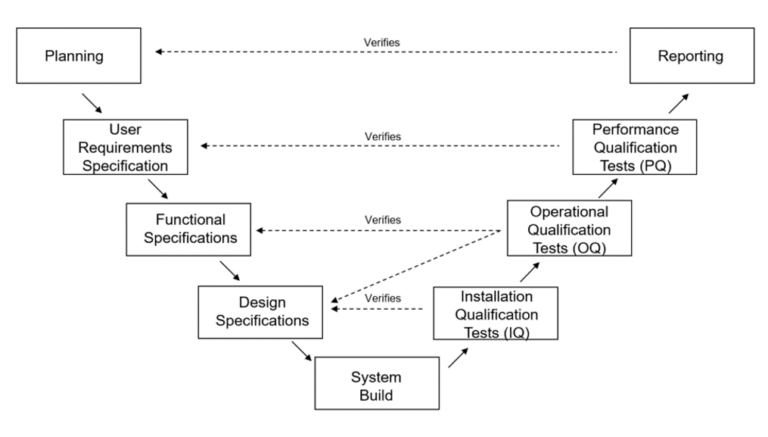
La calificación de equipos consiste en 3 procesos:
Calificación de Instalación (IQ)
Éste es el primer paso en el proceso de calificación de equipos. En esta fase se verifican las características de diseño del equipo y se asegura de que esté instalado correctamente.
Durante esta fase también se deben establecer programas y procedimientos de mantenimiento y calibración del equipo y dejar una evidencia documentada. Que constate que los equipos cumplen con los requerimientos exigidos por la normativa.
Calificación de Operación (OQ)
En esta fase de la calificación de equipos para dispositivos médicos se verifica que el proceso de fabricación cumpla con sus requisitos operativos. Las ejecuciones de prueba determinarán los parámetros operativos, los cuales ayudan a garantizar que el proceso sea reproducible.
Una vez aplicado estas pruebas, se genera un documento para dejar en evidencia que los dispositivos o equipos médicos cumplan con los estándares regulatorios y se ajustan a los requisitos que se exigen a nivel operativo.
Calificación de Equipos de Desempeño (PQ)
Es la última fase del proceso de calificación de equipos. Para aprobarla, el equipo debe funcionar en condiciones normales de operación y sus funciones serán desafiadas.
El propósito en este caso es demostrar que el proceso, bajo condiciones anticipadas, es capaz de producir un producto que cumple con todos los requisitos predeterminados de funcionalidad y seguridad.
Además de ello, se genera un informe donde hace constar el funcionamiento de los dispositivos o equipos es el óptimo y que estos están adaptados a las expectativas de la industria farmacéutica y que estos cumplan con el sistema de calidad exigido.
¿Por Qué es Importante la Calificación de Equipos para la Fabricación de Dispositivos Médicos?

Gracias a la calificación de equipos es posible garantizar un proceso de fabricación controlado y capaz de producir constantemente productos conformes y sin fallas.
Los dispositivos médicos deben ser evaluados y deben cumplir con los requerimientos regulatorios en todo su ciclo de vida, desde la fabricación hasta la distribución. Especialmente en aquellos productos que están clasificados de alto riesgo.
Este proceso de calificación es la forma de garantizar la calidad absoluta de los dispositivos médicos. Si requieres calificar tus equipos, comunícate con nosotros.
En Cercal Group somos consultores certificados. Brindando asesoría para el cumplimiento de las normativas regulatorias. Agenda tu cita.
Prevención de Contaminación Cruzada en Industrias Críticas: Estrategias Esenciales
Las industrias críticas como la farmacéutica, la de alimentos, laboratorios, así como clínicas y hospitales deben cuidar rigurosamente sus procesos y espacios para evitar riesgos como la contaminación cruzada. Esta es la primera causa de incidencias en las líneas de producción, por lo que es esencial abocarse a esta problemática para solucionarla.
La contaminación cruzada se produce cuando se transfieren elementos contaminantes de una sustancia a otra que pueden resultar perjudiciales para la salud. Existen tres formas de contaminación cruzada:
Contaminación Biológica
Causada por bacterias, virus, hongos.
Contaminación Química
Debido a moléculas, vapor, humedad.
Contaminación Física
Cuando se ocasiona por partículas.
La Calidad del Aire y su Incidencia en la Contaminación Cruzada
Los sistemas de ventilación son fundamentales para evitar o minimizar la posibilidad de transferencias de patógenos y otros elementos contaminantes. Es por esta razón que los sistemas de renovación del aire de las salas críticas como pabellones quirúrgicos o habitaciones de fabricación de medicamentos, deben estar diseñados para evitar la contaminación cruzada.
Teniendo en cuenta esto, es clave asegurar que los equipos de aire cuenten con la calificación de equipos que asegure el estricto control de los parámetros ambientales según el uso que tenga la sala. La norma ISO 14644-1 regula las salas limpias, y para seguir esta regulación los equipos de aire deben estar calificados para controlar la concentración de partículas contenidas en el aire.
Si se cuenta con la calificación de equipos correspondiente, será posible manipular productos y elementos con la seguridad de que el proceso, se lleva a cabo de forma apropiada, sin que resulte contaminado y que, a su vez, tampoco actúe como agente contaminante de otros productos o elementos.
¿Cómo Garantizar el Control del Aire en una Sala Limpia?
Es esencial implementar medidas para evitar la contaminación cruzada en las salas limpias mediante la calificación de equipos. La forma de hacerlo es llevando a cabo una supervisión periódica de equipos de aire.
Los sistemas HVAC deben tener un mantenimiento óptimo y ser inspeccionados con regularidad para que obtengan la certificación necesaria.
Somos especialistas en inspección de sistemas HVAC, y en certificación de salas limpias. Contáctanos y te brindaremos la asesoría que necesitas para cumplir con las normativas vigentes y garantizar la seguridad de tus espacios críticos.
Cercal Group: Excelencia en Calificación de Equipos para la Industria Farmacéutica
En Cercal Group, nos especializamos en servicios de calificación para la industria farmacéutica. Nuestro enfoque está en garantizar que tus equipos cumplan con las especificaciones establecidas y las normas de seguridad.
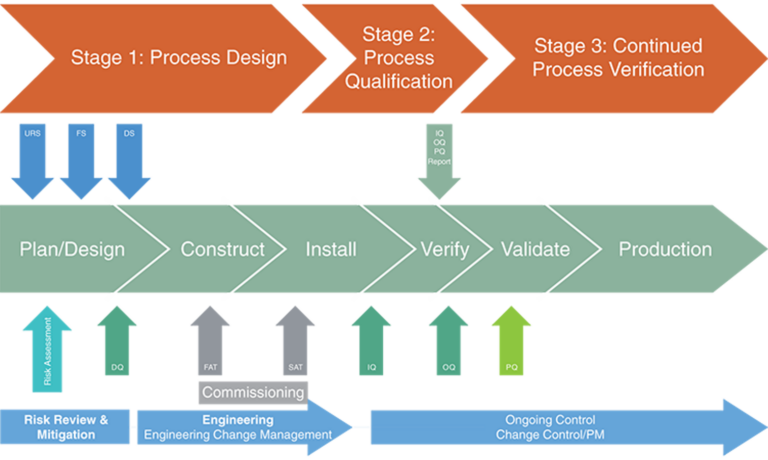
Ofrecemos una gama completa de servicios de calificación, desde la calificación de diseño hasta la calificación del desempeño. Nos aseguramos de que cada sistema crítico funcione dentro de los rangos de operación definidos y por periodos prolongados.
Nuestros servicios de calificación incluyen la validación del proceso y la verificación documentada. Esto asegura el control de calidad y la conformidad con las normas regulatorias.
Entendemos la importancia de prevenir riesgos en la producción. Por eso, nuestra calificación previas y la calificación de sistemas están diseñadas para identificar y mitigar cualquier desviación.
La calificación de diseño es el primer paso en nuestro proceso. Evaluamos los sistemas críticos para asegurar que cumplan con las expectativas de la industria farmacéutica.
Luego, procedemos con la validación del proceso, estableciendo parámetros definidos que garantizan la eficacia y seguridad de los equipos.
En Cercal Group, te ofrecemos estos servicios con el objetivo de mantener la integridad de tus operaciones.
Nuestra experiencia y dedicación en la calificación de equipos te proporcionan la confianza necesaria para operar eficientemente. Con nosotros, tu producción estará libre de contaminación cruzada y otros riesgos, asegurando productos de la más alta calidad para tus clientes.
Conclusión
La calificación de equipos es fundamental en el aseguramiento de la calidad del producto final. Este proceso no solo valida la eficacia de los equipos de producción, sino que también establece un marco para la gestión de calidad continua.
A través de actividades de validación meticulosas, se garantiza que los procesos de producción cumplan con las especificaciones técnicas y normativas de seguridad aplicables.
La validación de proceso, en particular, juega un papel crucial al evaluar la capacidad de los equipos para operar según los parámetros establecidos, asegurando productos de calidad.
El mantenimiento preventivo emerge como un componente esencial en la calificación de equipos. Este no solo prolonga la vida útil de los dispositivos de medición y producción, sino que también minimiza el riesgo de fallas que puedan comprometer la calidad del producto.
La ejecución del proceso, por lo tanto, se mantiene dentro de los límites de control, gracias a un análisis de riesgo proactivo y una planificación detallada.
En conclusión, la calificación de equipos es una piedra angular en la producción de calidad. Abarca desde la selección y diseño de los equipos hasta su validación y mantenimiento, asegurando que cada etapa del proceso de producción esté alineada con los estándares de calidad más altos.
Este enfoque integral no solo mejora la eficiencia y la seguridad de los procesos de producción, sino que también refuerza la confianza en los productos finales entregados al mercado.



One thought on “Importancia de la Calificación de Equipos para la Fabricación de Dispositivos Médicos”